打开文本图片集
[摘要] 目的 观察成人Still病(AOSD)的淋巴结病理形态特点,探讨其在AOSD诊断中的临床意义。 方法 对浙江省桐乡市中医医院病理科收治的4例AOSD患者的临床资料进行回顾性分析,并对其淋巴结活检及免疫组化标记结果进行观察分析。 结果 患者主要表现为体温升高、皮疹及关节痛等临床症状,肝脾及淋巴结肿大,外周血白细胞较正常水平升高,EB病毒,HIV及抗RNP抗体正常。患者淋巴结部分结构保存,副皮质区增宽,淋巴结主要呈增生性改变,增生细胞主要是免疫母细胞及Langerhans细胞,可见小淋巴细胞及组织细胞等散在分布,增生细胞核分裂象较多见,且异型性明显。免疫组化标记结果显示,免疫母细胞表达CD20及CD79α或表达CD3及CD45RO,Langerhans细胞胞质及胞核、高尔基区,CD1a和vementin胞质阳性,活化的淋巴细胞表达CD30,组织细胞表达CD68,CD15及ALK等均无表达。 结论 AOSD临床诊断不依赖于淋巴结活检,但淋巴结活检对AOSD的诊断具有重要的辅助价值,且肿大的淋巴结的免疫反应特点对AOSD的鉴别诊断也具有重要意义。
[关键词] 成人Still病;淋巴结;病理诊断;临床意义
[中图分类号] R542.22 [文献标识码] A [文章编号] 1673-7210(2013)10(a)-0096-04
不明原因发热最常见的原因是感染性疾病、炎性血管疾病、结缔组织疾病、恶性疾病等。在炎性血管疾病及结缔组织中,比例最高的是成人Still病(adult-onset Still"s desease,AOSD)。AOSD患者常表现为高热、一过性皮疹、关节炎及多器官受累等临床症状,常伴有肝脾淋巴结肿大及外周血白细胞增高[1],目前,对于其病因及发病机制尚不明确,可见于任何年龄,但以18~25岁人群多见,无性别差异。临床医师在诊断此病时多依靠患者病史及相关检查且常依赖病理诊断来进行排除性诊断。国内外有相关AOSD肿大淋巴结病理学改变的相关研究极其少见,缺乏明确诊断标准。本文回顾性分析AOSD在不明原因发热中所占的比例及其临床特点。旨在通过对4例AOSD患者的临床资料进行回顾性分析总结,以观察AOSD患者淋巴结形态特点,并探讨其在AOSD诊断中的临床意义,现报道如下:
1 资料与方法
1.1 一般资料
浙江省桐乡市中医医院病理科2005~2010年共收治4例AOSD患者,其中女3例,男1例,年龄18~30岁,患者均有无明显诱因发热,体温39~40℃,且其中2例患者采用药物治疗退热后,隔天再次发热,患者在入院时及后来均出现躯干及四肢等红色小皮疹,有痒感或伴其他部位疼痛。4例患者入院后均进行血常规检查,并行外斐试验、结核菌素试验及肥达试验等,试验结果显示,EB病毒、人类免疫缺陷病毒(HIV)及抗核糖核蛋白(RNP)抗体等均正常。
1.2 方法
4例患者标本采用10%的中性福尔马林固定,常规石蜡包埋切片,行HE染色,采用EnVision两步法进行免疫组化标记,所用标记抗体CD3、CD20、CD68、CD21、ALK、TIA-1、穿孔素及CD56等均购自泉晖公司,将已知阳性切片作为阳性对照组,将PBS代替一抗作为阴性对照组,阳性判断:棕黄色,无背景染色。
2 结果
2.1 眼观
4例患者淋巴结均有轻度肿大,直径0.5~2.2 cm,肿大的淋巴结与周围组织分界清楚,淋巴结之前也无明显粘连,质中等偏软,切面呈灰白色。
2.2 镜检
肿大的淋巴结正常结构得以保存,淋巴滤泡残存,淋巴样组织明显增生,其中可见成熟的小淋巴结胞、嗜酸性粒细胞等散在分布,还可见免疫母细胞及Langerhans细胞等,另外,可见核分裂象。其中Langerhans细胞在高倍镜下观察时呈肾形或椭圆形,细胞体积大,胞质轻度嗜酸性,核椭圆形或肾形,免疫母细胞高倍镜(400×)下观察时,细胞体积大,核大呈空泡状,伴有明显的中央核仁。本组4例患者中,2例以免疫母细胞为主,2例以Langerhans细胞为主,其中2例有上皮样毛细血管增生。
2.3免疫表型
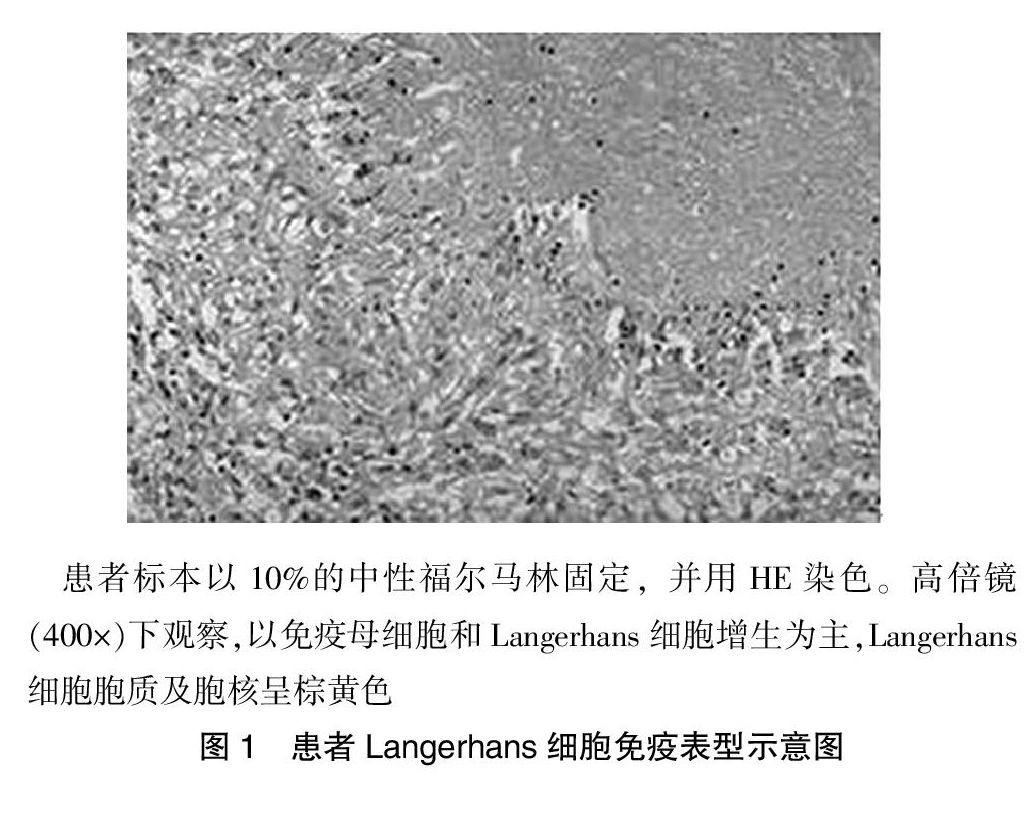
部分免疫母细胞表达CD20及CD79α,部分表达CD3及CD45RO;Langerhans细胞胞质及胞核呈棕黄色,高尔基区,CD1a和vementin胞质阳性;活化的淋巴细胞表达CD30,组织细胞表达CD68,CD15及ALK等均无表达。患者免疫表现见图1。
患者标本以10%的中性福尔马林固定,并用HE染色。高倍镜(400×)下观察,以免疫母细胞和Langerhans细胞增生为主,Langerhans细胞胞质及胞核呈棕黄色
2.4 淋巴结诊断
结合淋巴结活检显示的淋巴结形态学特点及患者临床表现,实验室检查结果,诊断为AOSD。
3 讨论
AOSD目前尚无统一的治疗方案,也无根治办法。治疗原则是尽早诊断、合理治疗缓解病情、防治并发症及预防复发。对于仅表现为发热和关节症状,而不伴有脏器损伤的轻症患者可仅给予非甾体类消炎药治疗,但绝大部分患者需加用糖皮质类固醇激素。糖皮质激素免疫抑制作用较强,能短时期内改善病情,因此,本研究认为应早期应用糖皮质激素。AOSD的预后谱较广,部分患者一次发作缓解后不再发作,约50%有自限性,部分缓解后易反复发作,有的呈慢性持续活动。也有部分患者因关节受累严重而导致关节畸形,另有极少数患者出现严重的并发症死亡。
AOSD在临床上并不常见,同大多数风湿性疾病一样,其病因至今不清楚,研究认为AOSD的发生可能与遗传、感染、细胞因子等有关。对于AOSD的诊断目前一般采用1992年日本AOSD研究委员会的诊断标准[2]:①主要指标:体温升高≥39℃且持续超过1周,关节持续疼痛超过2周,血常规检查显示WBC≥15×109/L,患者有典型皮疹。②次要指标:肝脾及淋巴结肿大;咽痛;肝功能异常;ANA阳性,RF阴性。③排除:恶性肿瘤,感染性疾病及其他风湿病。在排除以上标准上列出的其他疾病的前提下,若患者满足以上5项或5项以上指标,且其中至少有2项为主要指标即可诊断为AOSD。
由于ASOD为临床排除性诊断,临床医师一般不需进行淋巴结活检,但在患者症状体征不典型时,临床医师则常需要行淋巴结活检,以排除恶性淋巴瘤及结核等疾病,同时验证自己的诊断[3]。目前,对于ASOD淋巴结病理学改变尚无明确的诊断标准,有学者研究结果显示,Langerhans细胞组织细胞增生症时,AOSD可表现为局灶性Langerhans细胞增生[4]。也有学者通过对12例AOSD淋巴结的分析,将AOSD患者淋巴结病理学改变分为4类[5]:①大部分患者淋巴结副皮质增生,且血管增生最为显著,伴有T和(或)B免疫母细胞增生且体积增大,伴有炎细胞及反应性小淋巴细胞浸润。②部分患者淋巴结副皮质增生,伴有S-100阳性细胞浸润及窦组织细胞增生。③部分患者可见T免疫母细胞高度反应性增生,且常多见核分裂象。④部分患者淋巴滤泡增生。从本组研究结果显示,AOSD患者副皮质区增高,但淋巴结结构部分保存,免疫母细胞及Langerhans细胞增生,可见核分裂象,与文献报道的AOSD淋巴结病理学改变特点相符,而本组4例患者有体温升高、皮疹及关节疼痛等临床症状,体征检查显示淋巴结不同程度肿大,另外,血常规检查结果提示外周血白细胞计数超出正常值上限,均符合AOSD临床诊断标准。由于AOSD临床表现复杂,因此常需与其他多种疾病如感染、肿瘤及自身免疫性疾病等鉴别,需要排除上述疾病后才能做出诊断[6]。除此以外,部分患者淋巴结结构完全消失,其内免疫母细胞和(或)Langerhans细胞增生,细胞异型性明显,且较常见核分裂象,在不清楚患者病史或对AOSD患者淋巴结改变认识不足的情况下,病理医师应注意与Langerhans细胞组织细胞增生症、传染性单核细胞增多症、淋巴瘤及组织细胞坏死性淋巴炎相鉴别[7]。通过进行本组研究并结合相关文献报道,本研究认为虽然AOSD患者淋巴结改变不具有特异性,但是其反应性增生性改变对AOSD的诊断仍具有重要提示意义,患者淋巴结的反应性增生形式多样,可能与患者病程不同或者对免疫刺激的反应不同有关[8]。
本病是在1971年首先进行报道的,在1973年正式命名,在1987年后命名为AOSD,即:成人斯蒂尔病。该病是一种独立的疾病,病例的发病年龄大多在19~37岁,发病患者中女性较多,这与国外此类报道的文献相符。本病目前发病病因尚不明确,病理机制也不明晰,部分学者认为该病的发生于EB病毒感染及其炎症反应相关,大多数学者认为该病属于变态反应,而感染在该病的急性期有明显的作用,但是变态反应在整个病程中起主导作用,临床中主要表现为关节炎、关节痛、皮疹、高热等主要症状,而感染在其急性期起到诱因的作用[9]。变态反应在患者的整个病程起着主导作用。患者的临床表现为咽痛、咳嗽、淋巴结肿大、肌痛、浆膜炎、肝脾肿大等。临床表现的复杂性是该病的主要特点。而皮疹大多会在患者出现发热症状后产生。患者关节的疼痛程度与患者皮疹形态有较大差异,在本组试验中,患者在急性活动期有白细胞、C反应蛋白异常升高、血沉、细菌培养,ANA、RF检测多为阴性以外,血清铁蛋白(SF)也有明显的异常升高,因而要高于一般的感染及普通人[10]。
AOSD患者的典型体温要高于39℃,患者每天会出现1个或以上的高峰,部分患者甚至出现持续性高峰。患者高峰的特征是:当患者发热或出现不适时,一般状况并未出现不适。典型的AOSD患者皮疹容易消失,患者大多会出现斑丘疹或淡红色的斑疹。随着患者的发热高峰出现在四肢及躯干,发热退去后,患者的皮疹就会消失,这种现象在其他病中并未发现[11]。
对患者进行骨髓穿刺及淋巴活检可以检出,AOSD患者虽然没有特异性,但是病例中应排除淋巴瘤等疾病,而对于反复发作的患者,应及时地对其进行治疗,但是疗效尚不显著,因而要对患者进行淋巴结活检及反复的骨髓穿刺。本病无特异性的实验室进行检查,因而在患者的急性活动期,患者会出现血沉、CRP、白细胞增高的情况,最主要的是,患者体内的血清铁蛋白增高异常迅速,显著高于一般的传染性疾病及结缔组织疾病。因此,患者的血清铁蛋白的上升是诊断该病的有力依据。血清铁蛋白作为AOSD活动期的标志物,该比值早缓解期及活动期都较低。由于AOSD诊断难点较多,因而在确诊前一定要率先排除感染性疾病及肿瘤、其他免疫疾病等,并且要排除布氏杆菌感染[12]。
AOSD目前病因尚不清晰,但是临床上普遍认为该病与感染相关,尤其与病毒、链球菌感染相关。临床上主要表现为急性炎症过程。患者出现免疫异常症状,并且有明显的全身受累表现。治疗中,肾上腺皮质激素有效但抗生素无效,因而被称之为变态行反应,但是目前仍未发现感染的直接证据。一些研究还表明,细胞因子在AOSD的发病中也占有显要位置。另一部分研究显示,患者疾病的发病与白细胞抗原相关,并且许多病原体都会参与。患者的症状不够典型,表现发杂且多样,因而需要进行反复的检查,以排除肿瘤、感染性疾病及其他结缔组织疾病,因而在临床上容易出现漏诊及误诊。针对该种诊断,国内外出现了多个诊断的标准,但是目前仍然缺乏统一的判断标准。王臻等[4]对4种最常用的标准进行临床验证,认为Yamaguchi标准的敏感度最高为78.6%,准确率为87.1%,推荐Yamaguchi标准用于国内目前临床诊断较为合适。本研究也采用了Yamaguchi诊断标准。
综上所述,临床上对AOSD的诊断并不依赖淋巴结活检,但淋巴结过度的免疫反应表现对AOSD的诊断仍然具有一定的价值,同时,可通过进行淋巴结活检,以排除其他淋巴结病变,对AOSD的准确诊断也具有重大意义。
[参考文献]
[1] 李丽,李响,栾九松,等.成人Still病63例临床诊治分析并文献复习[J].中国全科医学,2011,14(1):99-101.
[2] 雷小妹,李守新.血清铁蛋白检测在成人Still病诊断和治疗中的临床价值[J].临床内科杂志,2006,23(10):667-669.
[3] 莫祥兰.富于免疫母细胞型成人Still病性淋巴结病2例病理分析莫祥兰[J].山东医药,2010,50(43):82-83.
[4] 王臻,姜林娣.4种成人Still病诊断标准的临床验证[J].复旦学报:医学版,2010,37(5):552-554.
[5] 孙乐栋,曾抗,周再高,等.成人Still病31例临床分析[J].中国皮肤性病学杂志,2006,20(2):93-94.
[6] 樊慧珍,于化鹏,杨振峰,等.成人Still病45例临床分析和诊治体会[J].广东医学,2005,26(12):1687-1689.
[7] 马丽,钳志晶,赵孟君,等.成人Still病与急性重度肝损害[J].中华风湿病学杂志,2007,11(8):489-491.
[8] 朱新林,左菊英,杨德辉,等.成人still病20例临床分析[J].实用医学杂志,2006,22(11):1285-1286.
[9] 张奉春,杨慧君,佟胜全,等.血清铁蛋白在斯蒂尔病中的临床意义[J].中华风湿病学杂志,2001,5(4):125-126.
[10] 梅开勇,林汉良,魏振青,等.22例淋巴结朗格汉斯细胞组织细胞增生症病理学分析[J].中华血液学杂志,2004,25(1):54-56.
[11] Vignes,Wechsler B,Amoura Z,et al. Intravenous immunoglobulin in adult Still"s disease refractory to non- steroidalanti-inflamma-torydrugs [J]. Clin Exp Rheumatol,1998,16(3):295-298.
[12] Masson C,Le Loet X,Liote F,et al. Adult Still"s disease. Part 2. Management,outcome,and prognostic factors [J]. Rev Rheum Engl Ed,1995,62(11):758-765.
(收稿日期:2013-05-05 本文编辑:张瑜杰)
